- Latest news▼
-
15:32, 26 апреля ESCMID: новый метод очистки воздуха ультрафиолетом защитит мир от новой пандемии

-
13:44, 26 апреля JAD: долгий сон на выходных снижает частоту проявлений депрессии на 64%

-
08:43, 26 апреля Открыты ферменты, превращающие разные группы крови в первую

-
01:20, 26 апреля Ученые выяснили что нужно есть, чтобы быть умным

-
23:42, 25 апреля eLife: освещенность стимулирует когнитивные способности у людей

-
21:23, 25 апреля В США проводятся испытания лекарства против старения на людях

-
21:06, 25 апреля Хирургам МЦ «Наири» удалось сохранить селезенку при большой аневризме селезеночной артерии

-
19:41, 25 апреля В Ереване состоится международный гибридный симпозиум «Аллергология и Иммунология»

-
19:36, 25 апреля Минздрав России зарегистрировал первый в мире препарат для лечения болезни Бехтерева

-
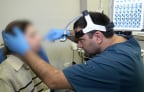
17:31, 25 апреля JAMA: у пациента выросли длинные кудрявые ресницы из-за химиотерапии
-
13:39, 25 апреля В Польше зафиксировали резкий рост заболеваемости корью
-
11:45, 25 апреля В Горисе будет создана станция переливания крови
-
11:08, 25 апреля В Республике Конго объявили эпидемию оспы обезьян

-
09:13, 25 апреля Сложная операция в МЦ «Бест Лайф»: пациенту одновременно поставили несколько стентов и эндографтов

-
08:31, 25 апреля OU: отказ от курения в 4 раза повышает шансы на излечение от рака гортани

Все материалы
Как заставить организм бороться с раком? – в свет выходит книга о передовом направлении в онкологии

В издательстве «Бомбора» выходит книга медицинского журналиста Чарльза Гребера о передовом направлении в онкологии. ТАСС опубликовало краткое содержание, написанное автором.
Избавиться от опухоли можно тремя способами: удалить, вытравить или облучить. Методы эти оставляют желать лучшего. Рак остается второй самой распространенной причиной смерти в мире: по данным Всемирной организации здравоохранения, в 2018 году из-за этого умерли 9,6 млн человек.
Совсем недавно оказалось, что этот новый, четвертый способ лечения все-таки действует, пускай пока он далек от совершенства, а иммунологам Джеймсу Эллисону и Тасуку Хондзё, как и предрекал Гребер, присудили Нобелевскую премию. Именно о нем пишет Чарльз Греббер в своей книге «Открытие. Новейшие достижения в иммунотерапии для борьбы с новообразованиями и другими серьезными заболеваниями».
«При определенных условиях человеческая иммунная система умеет распознавать и убивать рак. И возможно, иммунный подход это самый лучший способ получить лекарство. Но по какой-то причине он не работал. Онкологи-иммунологи много лет пытались понять, в чем дело.
Иммунная система, как и рак, — это гибкая, адаптивная и эволюционирующая система. Рак уже доказал свою способность восстанавливаться после прямых атак лекарствами или радиацией — эта уникальная, сбивающая с толку, способность сейчас известна нам как «побег». Даже если лекарство успешно атакует рак, опухоль мутирует и избегает атаки. Выжившие клетки возвращаются с новой силой и уже неуязвимы для прежних лекарств. Эта способность к мутации определяющая для рака. Но адаптивность и мутации являются определяющими и для иммунной реакции.
Иммунная система отлично справляется с большинством незваных гостей в кровеносной системе: она находит больные клетки, атакует их и убивает. Рак — это больная клетка, мутант из нашего собственного организма, который не может перестать расти. Так почему же иммунитет не реагирует на рак так же, как, например, на простуду? Почему именно иммунная реакция на рак не такая, как на все другие болезни, и как ему удается избежать сложнейшей паутины ловушек и разведчиков, следопытов и убийц, патрулирующих периметр эпидермиса и курсирующих по кровеносной системе? Большинство ученых считали, что иммунная система просто не умеет распознавать рак как чужеродную («не свою») клетку, потому что он слишком похож на нормальные, здоровые клетки.
Объединение упрямых онкологов-иммунологов возражало. Они считали, что рак каким-то образом умеет прятаться от «охотников» и «следопытов» иммунной системы, обманывать их. И они оказались правы. Рак пользуется разнообразными уловками, чтобы избежать уничтожения.
Всего несколько лет назад эта точка зрения считалась смехотворной большинством специалистов по раку, и даже немногие иммунологи, которые до сих пор держались за нее, постепенно начинали считать ее безнадежной. Но в 2011 году несколько важных новых открытий, прорывов в исследовании рака, наконец-то помогли идентифицировать некоторые недостающие части «мозаики», которые мешали иммунной системе распознавать и атаковать рак.
Некоторые тайны иммунной системы наконец удалось вывести на свет божий; о существовании и роли T-лимфоцитов как «серийных убийц» чужеродных клеток знали довольно давно. Были идентифицированы конкретный «ключ зажигания» для иммунной реакции — рецептор на T-клетке, который «включался», или активировался, распознавая уникальные белковые отпечатки (антигены) на больных или зараженных клетках, а также механизм работы амебообразных дендритных клеток, которые служат в иммунной системе своеобразными «обозными», доставляя антигены T-лимфоцитам, чтобы те учились их распознавать. С антигеном T-лимфоцит получает боевой приказ: ему показывают «портрет» врага, уникальные поверхностные белки больной клетки, и отправляют искать и уничтожать эти клетки.
Но, конечно же, поскольку это человеческая иммунная система, все не может быть так просто.
Иммунная система сильна и, следовательно, опасна. Правильное включение иммунной системы для борьбы с патогенами поддерживает в вас здоровье. Но вот неправильная поспешная иммунная реакция на собственные клетки организма это уже аутоиммунная болезнь. На клеточном уровне решения, от которых зависят жизнь и смерть, принимаются с высоким уровнем избыточной безопасности.
По-настоящему взломан оказался код после открытия второго сигнала, необходимого для активации T-лимфоцита. Но это открытие оказалось сюрпризом.
Ученые искали второй сигнал, еще одну кнопку «старт», которая играет роль педали газа для T-лимфоцита и запускает целый каскад реакций, которые мы называем иммунным ответом и которые завершаются гибелью врагов.
Тормоз, который называется CTLA-4, полезен для предотвращения аутоиммунных атак на «свои» клетки. Эллисон обнаружил, что рак использует этот тормоз для своих целей. CTLA-4 — это не ключ, а выключатель, контрольная точка. Рак пользуется тормозом, встроенным в иммунную систему, чтобы выживать и процветать. Разработав лекарство (антитело), которое прикреплялось к «тормозу» и блокировало его, ученые не дали T-лимфоциту заглохнуть, а опухолевой клетке — остановить работу иммунной системы.
В метафорическом смысле этим открытием они сняли ногу рака с педали тормоза иммунной системы.
Открытие CTLA-4 запустило ход других кусочков иммунной «мозаики», в том числе спровоцировало активные исследования и клинические испытания других, более новых ингибиторов контрольных точек. Главными звездами стали антитела к PD-1, которые воздействуют на «секретное рукопожатие» запрограммированной клеточной смерти (PD) со стороны T-лимфоцитов, и к PD-L1, блокирующие его со стороны раковой опухоли.
Эти лекарства совершенно изменили ситуацию с лечением нескольких типов рака», - отмечается в книге.
Следите за NEWS.am Medicine на Facebook и Twitter
- Видео
- Календарь событий
- В Ереване состоится международный гибридный симпозиум «Аллергология и Иммунология»
- В Ереване состоится первая армяно-германская конференция «Весенняя школа сердечной недостаточности»
- В Армении впервые проведена аллогенная трансплантация костного мозга при гематологическом злокачественном заболевании
Все материалы
- Архив
- Самые читаемые
месяц
неделя
день
- Специалист о результатах мониторинга инспекции по безопасности питания: Считайте, что онкоцентр ждет вас 1709
- Следующую пандемию, скорее всего, спровоцирует грипп – ученые 1231
- Ученые выяснили, почему алкоголь вызывает отключение сознания 1160
- Бывшая модель чуть не умерла, пытаясь вылечить рак с помощью найденной в Интернете соковой диеты 1091
- Некоторые препараты, назначаемые для лечения деменции, вызывают серьезные побочные эффекты – исследование 1072
- Российские ученые усовершенствовали методы диагностики аутизма у детей 1037
- Сильная тяга к сладкому может быть вызвана одиночеством – исследование 1030
- Сложная операция в МЦ «Бест Лайф»: пациенту одновременно поставили несколько стентов и эндографтов 1027
- Ученые обнаружили пациента, перенесшего самую длительную из известных на сегодняшний день инфекций COVID-19 1015
- Учёные признали выпечку и недосып опаснее алкоголя 1009
- Ученые разрабатывают новый метод безопасного стимулирования иммунных клеток для борьбы с раком 1007
- MedicalXpress: веганская диета не приводит к дефициту питательных веществ 965
- Анализ крови может определить, кто подвержен риску развития рассеянного склероза – ученые 958
- В продуктах детского питания известной фирмы нашли нездоровое количество сахара 910
- Британские ученые хотят обучиться ранней диагностике болезни Альцгеймера 909
- Опрос